体温の中枢調節の基本原理
名古屋大学大学院医学系研究科統合生理学
講師
中村 佳子
講師
中村 佳子
私達はラットを用いて、視床下部の視索前野に存在するプロスタグランジンEP3受容体発現ニューロンが体温調節の司令塔であることを突き止め、このニューロン群が出す恒常的なGABA作動性の抑制信号の強さを変えることによって体温が上下自在に調節されることを証明しました。
人間を含む哺乳類の体温は外気温が変化してもほぼ一定に37°C付近に保たれますが、平熱域から逸脱すると生命が維持できなくなることから、体温調節は生命活動の基盤的な機能です。脳の体温調節中枢は視床下部の視索前野にあり、感染時には発熱を起こす中枢でもあります。しかしながら、体温の調節司令を担う視索前野のニューロン群や調節メカニズムの動作原理は不明でした。そこで私達は、感染時に産生される発熱メディエーターであるプロスタグランジンE2(PGE2)の受容体、EP3を発現する視索前野ニューロン(EP3ニューロン)に着目し、平常の基本的な体温調節における機能を調べました。
ラットを気温36°Cの暑熱環境に置くと、4°Cの寒冷環境や25°Cの室温に置いた場合と比べて、神経の活性化マーカーであるFosを発現するEP3ニューロンが増加しました。一方、PGE2を脳内に投与すると、発熱が起こるとともに、暑熱によるEP3ニューロンの活性化が抑制されました。このことから、EP3ニューロン群は環境温度や感染の情報を受容して活動が変化することがわかりました。次に、EP3ニューロン群特異的な遺伝子導入を可能にする遺伝子組換えラットを作製し、EP3ニューロン群を蛍光標識したところ、熱の産生などの交感神経反応を駆動する視床下部背内側部に多数の神経終末が観察されました。その終末から放出される神経伝達物質を調べると、興奮性の神経伝達を担うグルタミン酸よりも抑制性の神経伝達を担うGABA作動性ニューロンのマーカーを含有する神経終末が圧倒的に多く見つかりました。また、電気生理学的な解析から、これらの神経終末がGABAを放出することも確認されました。化学遺伝学の方法を用いてEP3ニューロン群を活性化すると熱放散が促進され、体温が低下した一方、抑制すると褐色脂肪組織の熱産生が起こり、体温が上昇しました。ラットを暑熱環境に2週間置き、EP3ニューロン群の長期的な機能変化を調べると、GABA作動性の神経終末の割合が増加したことから、EP3ニューロンはGABAを放出する神経終末を増やすことで効率的に熱産生を抑制し、暑熱耐性を向上させていることが示唆されました。
本研究によって、視索前野のEP3ニューロン群は常に抑制性のGABA作動性信号を送り、その抑制の強さを変えることによって交感神経出力を制御し、体温を両方向性に調節することがわかりました。これらの実験結果から、体温調節の司令塔であるEP3ニューロンからの恒常的な抑制信号のトーンが体温を決定しているものと考えられます。
<掲載ジャーナル>
Prostaglandin EP3 receptor-expressing preoptic neurons bidirectionally control body temperature via tonic GABAergic signaling
Nakamura Y, Yahiro T, Fukushima A, Kataoka N, Hioki H, Nakamura K.
Science Advances 8 (51): eadd5463, 2022.
https://doi.org/10.1126/sciadv.add5463
Nakamura Y, Yahiro T, Fukushima A, Kataoka N, Hioki H, Nakamura K.
Science Advances 8 (51): eadd5463, 2022.
https://doi.org/10.1126/sciadv.add5463
<図の説明>
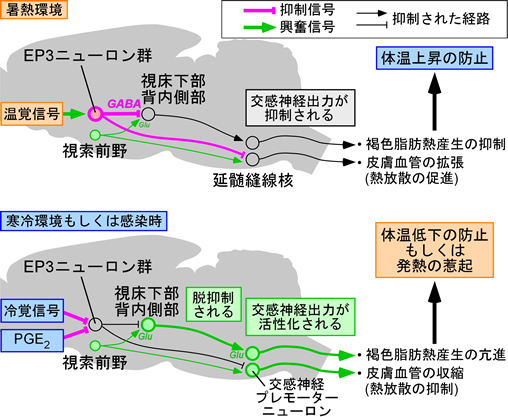
体温調節の基本原理
上図:
暑熱環境では、皮膚から温覚入力を受けて視索前野のEP3ニューロン群の活動が高まる。その結果、視床下部背内側部などの交感神経駆動脳領域へのGABA作動性の抑制信号が強まることで交感神経出力が弱まるため、皮膚血管の拡張を通じて熱放散が促進されるとともに熱産生が抑制され、体温の上昇を防ぐ。
下図:
寒冷環境あるいは感染が起こった場合、皮膚からの冷覚入力あるいは発熱時に産生されるPGE2をEP3ニューロン群が受容すると、その神経活動が抑制されるため、恒常的なGABA作動性の抑制信号が弱まる。その結果、交感神経駆動脳領域への抑制が解除(脱抑制)されて交感神経出力が亢進することで、褐色脂肪組織の熱産生が起こるとともに熱放散が抑制され、体温低下の防止あるいは体温上昇(発熱)が起こる。脱抑制された交感神経駆動脳領域の神経興奮は、視索前野を含めた複数の脳領域からのグルタミン酸(Glu)作動性入力が駆動すると考えられる。
<研究者の声>
本研究は神経終末の伝達物質を同定するために8万個以上のシナプス様構造を一つずつ目で見て数え、視索前野の細胞は、それ以上の個数を数えてマッピングし、今回の結果を得ました。この様な実験は時間がかかりますし、動物作製開始から様々な技術的困難もあり、13年かかって本研究を論文発表するに至りました。短期的な成果や論文数を求められる時代ですが、こうした時間のかかる研究に理解を示し、安心して研究に集中できる環境を与えて下さった中村和弘教授、研究の場を与え研究結果が出ることを楽しみにして下さっていた京都大学大学院医学研究科金子武嗣教授、実験にご協力下さった共著者の皆様、そしてラボメンバーに感謝いたします。





