2021年度塚原仲晃記念賞受賞者 松田 憲之 先生 受賞の言葉
松田 憲之 (東京医科歯科大学 難治疾患研究所 機能分子病態学分野 教授)
このたび、遺伝性潜性パーキンソン症候群(以降は遺伝性PDと記載)の原因遺伝子産物であるPINK1(セリン・スレオニンキナーゼ)とParkin(ユビキチン連結酵素)の研究に対して、塚原仲晃記念賞という名誉ある賞をいただけたことを大変に光栄に思っております。
もともと私は大学院生時代にRma1(RING finger with Membrane Anchor 1) というRING fingerモチーフを有するタンパク質の解析を行なっていました。RMA1遺伝子を単離したのは修士課程1年の時でしたが、その機能解析は遅々として進まず、当時の所属研究室の指導教官であった安楽泰宏先生・中野明彦先生の不安は並々ならぬものがあったかと思います。転機になったのは、1999年にRING finger モチーフがユビキチン連結酵素 (E3) のコンセンサス配列であることが示唆されたことでした。すぐにでもRma1のE3活性を調べたかったのですが、そうはいってもRma1はHisタグやGSTタグでは精製ができずに、やっと精製タンパク質を手にしたのはMBPタグを用いてからでした。さらに困ったことに、当時はユビキチン化に必須な因子群 (ユビキチン, E1, E2) が手元にありません。そこでHershko博士らの古典的な論文を参考に、in vitro translation 用に市販されているウサギ網状赤血球溶解物をユビキチン化関連因子群の代用品として用いるという荒技でin vitro再構成を試みました。今にして思えば、驚くほど荒っぽい実験ですが、それでもMg2+ATP存在下でMBP-Rma1と網状赤血球溶解物を反応させるとユビキチン化が再構成されて、MBP-Rma1の分子量がladder状に劇的に上昇しました。このデータが、その後のParkinの機能解析につながる、私のユビキチン研究の原点ともいえるものです。
この研究を通じてユビキチン研究の泰斗であった田中啓二先生との接点ができまして、2004年頃から田中研でParkin(Rma1と同様のRING finger タンパク質)の研究を始めました。ParkinのE3活性を細胞内で明瞭に観察できるようになるまでに、それから4年程かかりましたが、2010年には“通常時のParkinは不活性型であり、損傷ミトコンドリアに特異的に局在するPINK1によって活性型酵素に変換される”というシステムの大枠を見出すことができました。
「ParkinのE3活性を観察する」と言うのは簡単ですが、実は基質がわからない状態でE3酵素の活性を観察するのはなかなか難しいです。最も簡単なのは自己ユビキチン化活性を観察することですが、内在性ParkinやHAなどの小さなTagの付いたParkinの自己ユビキチン化を観察するのは至難の技で、E3活性の観察にはGFPやMBPなどリジン残基が豊富な大型のTagをParkinに付加することが必要です(これは実際に観察可能なE3活性が、自己ユビキチン化ではなくて、近傍偽基質に対する分子内ユビキチン化に由来するからです)。さらに、ユビキチン化を明瞭に観察するためには、NEMのような脱ユビキチン酵素阻害剤の添付が必要ですし、検出の際に使用するモノクロ抗体を正しく選択しないと、ユビキチン化によって抗原がマスクされてバンドが検出されなくなることもあります。このような“自然界の神様がしかける様々な罠”を避けて進むためには、Rma1の解析がうまくいかずに苦労していた頃の経験が役に立ちました。
今、この文章を読んでいる若手の方で研究がうまくいかずに苦労している方がいるかもしれませんが、試行錯誤を繰り返した時の苦労はきっと将来の糧になるから心配しないで!と言いたいです。私など大学院生の頃は指導教官に雷を落とされ続けて、避雷針3号という渾名を付けられたこともありましたし、3年では博士号を取ることができずに博士課程4年目を経験しています。でも、その当時の苦労があったらからこそ、上記のようなParkinの罠に嵌らずに済んだと思うのです。
いずれにせよ、GFP-Parkinの自己ユビキチン化(正確にはGFPを擬基質とする分子内のユビキチン化)を手掛かりに、ParkinがE3として働くためにPINK1が必須であること(JCB 2010)、PINK1の自己リン酸化がその機能に必須であること(Nature Commun 2012)、PINK1はユビキチンをリン酸化するキナーゼであり、リン酸化ユビキチンがParkinの活性化因子として機能すること(Nature 2014)、同時に損傷ミトコンドリア上で形成されるリン酸化ユビキチン鎖がParkin受容体として働くこと(JCB 2015)、などを解明しました。さらに、PINK1/Parkinの触媒するユビキチン鎖の意義を調べる過程で、Parkinが付加したユビキチン鎖をOptineurin (OPTN) が認識して、さらにOPTNがATG9(膜の供給に重要なオートファジー関連因子)と相互作用することで損傷ミトコンドリアを標的とするオートファジー(マイトファジー)を誘導すること(JCB 2020)、などがわかってきました。一連の成果から、(1) PINK1とParkinの触媒するユビキチン鎖がシグナルとなって損傷ミトコンドリアの近傍で de novo にオートファジーの種(隔離膜)が形成されて、(2) 損傷ミトコンドリアがマイトファジーを介して除去されるが、(3) PINK1やParkinの変異によってこの機構が破綻すると遺伝性潜性PDの発症につながる、という仮説を考えています(図1)。今後も引き続き、遺伝性PDの原因遺伝子の機能解析から、病気の発症メカニズムに迫っていきたいと考えています。
末筆となりましたが、今回の受賞対象となりました“PINK1/Parkinシステムのマイトファジーにおける機構の解析”は、私一人の成果ではなくて、多くの方々との共同研究の賜物です。スペースの都合もあって全員のお名前を記載できないのですが、メンターとして長い間私を指導してくださいました東京都医学総合研究所の田中啓二先生をはじめ、共同研究者の皆様全員に心から御礼を申し上げます。
図1
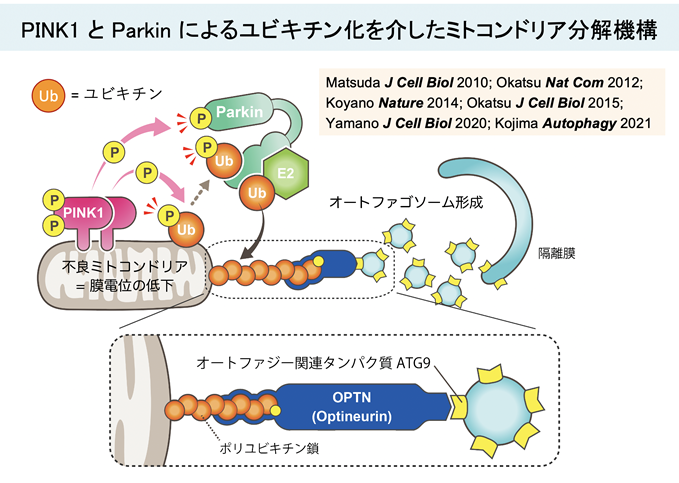
図の説明:
PINK1とParkinが協調して損傷ミトコンドリアをマイトファジー分解に導く仕組みの模式図。
詳細は本文を参照。
詳細は本文を参照。

松田 憲之
略歴
2001年 東京大学大学院理学研究科にて博士号(理学)取得
2001年 理化学研究所(生体膜研究室) 基礎科学特別研究員
2002年 東京都臨床医学総合研究所 外部支援研究員
2006年 日本学術振興会 特別研究員PD
2007年 理化学研究所(ゲノム科学総合研究センター) 研究員
2008年 東京都医学総合研究所 研究員
2014年 東京都医学総合研究所 プロジェクトリーダー
2022年 東京医科歯科大学 難治疾患研究所 教授(現職)
2001年 理化学研究所(生体膜研究室) 基礎科学特別研究員
2002年 東京都臨床医学総合研究所 外部支援研究員
2006年 日本学術振興会 特別研究員PD
2007年 理化学研究所(ゲノム科学総合研究センター) 研究員
2008年 東京都医学総合研究所 研究員
2014年 東京都医学総合研究所 プロジェクトリーダー
2022年 東京医科歯科大学 難治疾患研究所 教授(現職)
Noriyuki Matsuda
Biography
2001 Ph.D. (Biological Sciences), University of Tokyo
2001 – 2002 Special Postdoctoral Researcher, Molecular Membrane Biology Laboratory, RIKEN
2002 - 2006 Postdoctoral Fellow, Tokyo Metropolitan Institute of Medical Science (TMIMS)
2006 - 2007 Postdoctoral Research Fellow of the Japan Society for the Promotion of Science (JSPS)
2007 - 2008 Senior Scientist, Systems and Structural Biology Center, RIKEN
2008 – 2014 Senior (2008-2011) or Chief (2008-2014) Researcher, TMIMS
2014 – 2022 Project Leader, TMIMS
2022 - present Professor, Medical Research Institute, Tokyo Medical and Dental University
2001 – 2002 Special Postdoctoral Researcher, Molecular Membrane Biology Laboratory, RIKEN
2002 - 2006 Postdoctoral Fellow, Tokyo Metropolitan Institute of Medical Science (TMIMS)
2006 - 2007 Postdoctoral Research Fellow of the Japan Society for the Promotion of Science (JSPS)
2007 - 2008 Senior Scientist, Systems and Structural Biology Center, RIKEN
2008 – 2014 Senior (2008-2011) or Chief (2008-2014) Researcher, TMIMS
2014 – 2022 Project Leader, TMIMS
2022 - present Professor, Medical Research Institute, Tokyo Medical and Dental University




